プレスリリース
中部大学応用生物学部応用生物化学科の鈴木孝征准教授のグループは名古屋大学細胞生理学研究センターの廣明洋子客員准教授、同大トランスフォーマティブ生命分子研究所(WPI-ITbM)の東山哲也教授らとの共同研究で、スプライシングの新しいしくみを発見した。
発表内容
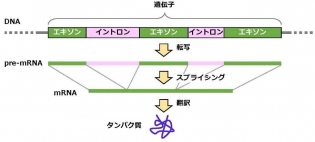
遺伝子からタンパク質がつくられる過程にはスプライシングというしくみがあり、これによって一つの遺伝子から複数のタンパク質がつくられ、遺伝子の機能を多様にしている(図1)。
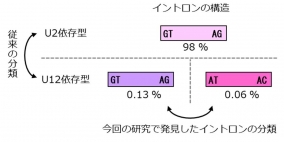
スプライシングで除かれる部分をイントロンとよび、これまでU2依存型とU12依存型の二種類に分類されていた(図2)。
U12型には末端の塩基配列が異なる二つのタイプ(GT-AG型とAT-AC型)があることが知られていたが、それらに機能的な差はないとされてきた。
鈴木准教授らは、植物研究のモデル生物であるシロイヌナズナを使ってDROL1遺伝子の機能を調べた。その結果、DROL1遺伝子の機能を失わせると、U12型のうちAT-AC型イントロンのみがpre-mRNAから除かれないことを発見した。AT-AC型イントロンは全体のごくわずかではあるが、そのスプライシングの異常は発芽を遅らせるなどの影響を与えた。
このことからDROL1遺伝子はAT-AC型イントロンをスプライシングする役割を持ち、その機能は植物の正常な発生に必要であることがわかった。
最近、ヒトでもAT-AC型とGT-AG型には違いがあることが報告されている。ヒトではスプライシングの異常は様々な病気の原因であることが突き止められ、AT-AC型イントロンのスプライシング異常も遺伝病の原因であることが示されている。
今後、DROL1遺伝子の基礎的な研究を進めていくと、ヒトの様々な病気の治療法の開発につながると考えられる。さらにイントロン両端の塩基配列とそれを認識するタンパク質との関係を詳しく調べれば、人為的なRNAの切断や組換えに応用することができる可能性がある。
研究成果の発表
今回の研究成果は2021年12月5日付の植物科学に関する英科学誌「ザ・プラント・ジャーナル(ThePlantJournal)」(電子版)に掲載された。
論文情報
Takamasa Suzuki, Tomomi Shinagawa, Tomoko Niwa, Hibiki Akeda, Satoki Hashimoto,Hideki Tanaka, Yoko Hiroaki, Fumiya Yamasaki, Hiroyuki Mishima, Tsutae Kawai,Tetsuya Higashiyama, Kenzo Nakamura.,“The DROL1 subunit of U5 snRNP in the spliceosome is specifically required to splice AT–AC-type introns in Arabidopsis”, ThePlant Journal.
本学の問い合わせ先
研究に関すること
鈴木孝征 (中部大学 応用生物学部 准教授)
E-mail:sem6875@fsc.chubu.ac.jp
電話:0568-51-6369(研究室直通)
報道に関すること
中部大学 学園広報部 広報課
Eメール:cuinfo@office.chubu.ac.jp
電話:0568-51-7638(直通)

