ポイント
- 魚に豊富に含まれ、脳機能に重要なドコサヘキサエン酸(DHA)(注1)は、脳内で主にリン脂質(注2)として存在します。DHAが結合するリン脂質には、その脂肪酸の結合位置が異なる構造異性体が含まれていますが、それらが脳内のどこに分布しているのかは、これまで明らかになっていませんでした。
- 本研究で用いた手法により、これまで区別できなかった「質量が同じリン脂質」を区別して可視化することに成功し、脳に特徴的に存在するDHA結合リン脂質sn位置異性体(注3)が、聴覚に関与する脳領域に多く分布していることを明らかにしました。
- 本研究で確立した手法は、質量が同じで構造のよく似た生体分子(sn位置異性体)を分離しながら組織内分布を可視化できる新しい解析技術であり、DHAの脳内取り込みや代謝解析をはじめ、さまざまな生体分子の体内動態や機能解明への応用が期待されます。
国立大学法人東京海洋大学(学長:井関 俊夫、以下「東京海洋大学」)の学術研究院食品生産科学部門の田中誠也助教、後藤直宏教授らは、魚に豊富に含まれ、脳機能に深く関連するドコサヘキサエン酸(DHA)を結合したリン脂質sn位置異性体のマウス脳内局在場所を世界で初めて可視化することに成功しました。
リン脂質には、同じ化学組成でありながら分子の構造がわずかに異なる「異性体」が存在します。しかし、これらの異性体を区別して観察することは従来の脂質イメージング(脂質の可視化法)では困難でした。
本研究グループは、サイクリックイオンモビリティー-質量分析イメージング(注4)という分析装置を用いて、通常では分離することが難しいリン脂質sn位置異性体を、装置内でイオンを30周させることで分離することに成功し、脳中リン脂質sn位置異性体分布を可視化しました。その結果、脳のみに特異的に存在する、DHAがリン脂質中のsn-1という位置に結合したリン脂質sn位置異性体が、脳内の聴覚に関わる場所に集まって存在していることを初めて明らかにしました。
本手法は、sn位置異性体を含む多様な分子の精密解析を可能にし、DHAの脳内動態解明をはじめとする生命科学研究の進展に貢献することが期待されます。
本研究は、日本ウォーターズ株式会社川瀬泰司氏、パクストン・タナイ氏、廣瀬賢治氏、福島大学農学群食農学類吉永和明准教授、桐明絢研究員、中部大学応用生物学部岩崎雄吾教授、大阪大学大学院理学研究科益田勝吉特任教授(常勤)と共同で行いました。
本研究成果は、2026年3月9日(米国東部時間)にAmerican Chemical Society(ACS)科学誌「Analytical Chemistry」のオンライン版で公開され、3月31日に出版されました。また本論文のインパクトの大きさが評価され、Supplementary Cover Artに選ばれました。
研究の背景と経緯
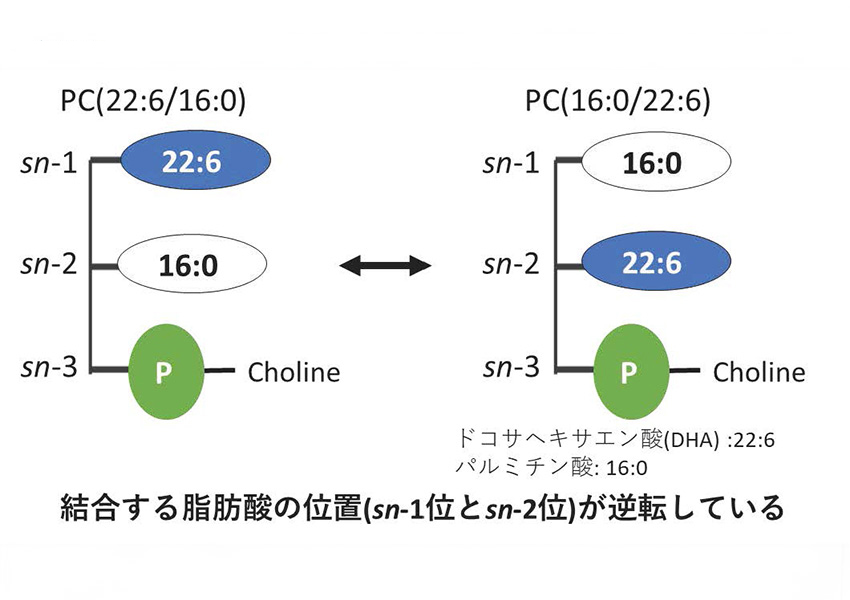
リン脂質はヒトや動物の細胞膜を構成する主要な成分であり、その分子内には2つの脂肪酸が結合しています。これらの結合位置の違い(sn-1位とsn-2位)によって、同じ分子組成でありながら構造が異なるsn位置異性体が存在します(図1参照)。また脳にはドコサヘキサエン酸(DHA)という機能性脂肪酸が豊富に含まれており、老化予防、アルツハイマー病やうつ病予防などとの関連が示唆されています。脳中のDHAは主にリン脂質に組み込まれて存在しますが、これまでの研究から、リン脂質の一種であるホスファチジルコリン(PC)(注5)には、血液や肝臓には見られない、脳に特有のDHA結合型sn位置異性体が特徴的に存在することが分かっています。具体的にはパルミチン酸(16:0)とDHA(22:6)からなるPCとして、PC(16:0/22:6) と PC(22:6/16:0)というリン脂質sn位置異性体が存在します。しかしこれらのリン脂質sn位置異性体が、脳の中でどこに分布しているのかは全くわかっていませんでした。脳における分布を調べることで、脳で特徴的なリン脂質sn位置異性体の生体内における機能を推測することができます。例えば脳に良いとされるDHA結合型のリン脂質sn位置異性体が海馬に集中して存在していた場合、脳機能の中でも記憶力などに関わる可能性が示唆されます。
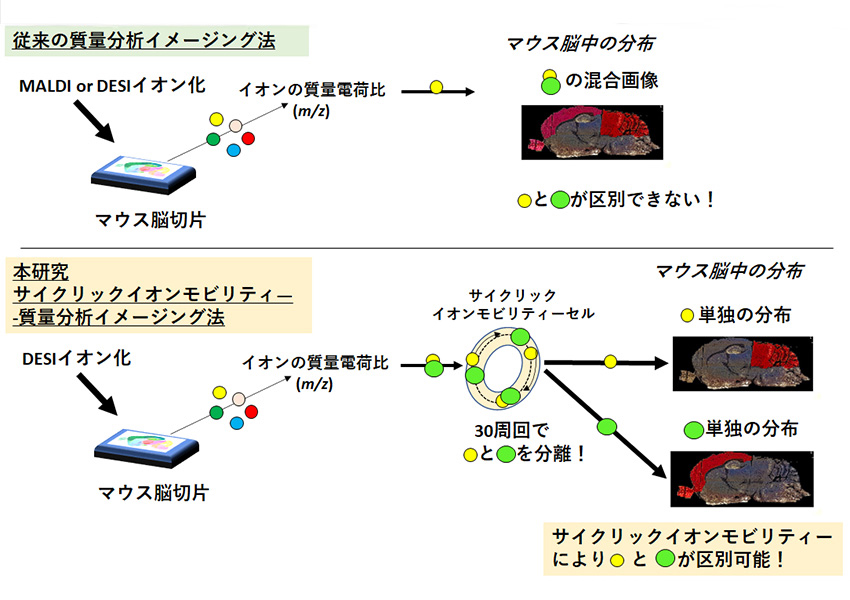
試料中の化合物の分布を調べる方法としては、質量分析イメージングを用いた可視化技術があります。質量分析イメージングは、試料にスプレー処理やレーザー照射を行うことで化合物をイオン化し、得られた質量ごとに地図のような画像を構成して、検出量に応じた色分けで可視化する技術です。従来の質量分析では、質量による識別しかできないため、質量が同じで構造が異なる分子(異性体)を区別することは困難でした。これを解決するために、イオンの立体構造の違いに基づいて分離する「サイクリックイオンモビリティー‐質量分析」という新しい分離技術が開発されました。この技術は、環状になっているセル内を、測定イオンを複数回周回させることで、複雑なペプチド構造やトリグリセリドなど、従来の方法では区別が難しかった分子の分離が可能になる技術です。しかし、これまでリン脂質のsn位置異性体のような、構造が非常に似通っている化合物を分離して可視化した報告はありませんでした。
研究の内容
上記の背景から、東京海洋大学の田中誠也助教らは日本ウォーターズ、福島大学、中部大学、大阪大学との共同研究で、マウスの脳に含まれるリン脂質sn位置異性体の可視化を試みました。田中らは、ドコサヘキサエン酸(DHA)が結合したリン脂質のsn位置異性体の標準品、PC(22:6/16:0)とPC(16:0/22:6)を合成し、サイクリックイオンモビリティー‐質量分析計を用いた分離手法の確立を行いました。その結果、図3で示すように、イオンモビリティーセル内を周回させることで、徐々に異性体の関係であるPC(22:6/16:0)とPC(16:0/22:6)が分離し、30周したところで良好な分離が得られました。
次に、確立した条件でマウス脳スライスについて分析し、検出されたイオン量に基づいて地図のような画像(イメージング画像)を作製しました。その結果、図4のようにPC(22:6/16:0)とPC(16:0/22:6)の脳内分布で明確な違いが見られ、PC(22:6/16:0)は下丘(注6)(聴覚に関わる脳領域)、PC(16:0/22:6)は嗅球(嗅覚に関わる脳領域)や小脳、脳幹(呼吸や自律神経系に関わる脳領域)に分布していました。これにより、分子量が同一でも脂肪酸の結合位置が異なるリン脂質sn位置異性体は、それぞれ脳内分布が明確に異なることが初めて明らかになりました。
さらに今回対象としたDHA結合リン脂質は脳内での半減期(化合物が半分になるまでの時間)が長く、長期間脳に留まることが知られています。しかし、食事から摂取されたDHAが、このような脂肪酸の結合位置が異なるリン脂質sn位置異性体に実際に組み込まれているのかは不明でした。そこで、安定同位体(注7)標識DHA(分子量が+3で、通常のDHAと同一の化学的性質をもつもの)を用意し、マウスに5日間連続で摂取させました。その結果、食事由来のDHA(22:6)が脳に取り込まれ、PC(22:6/16:0)は下丘に、PC(16:0/22:6*)は嗅球に多く蓄積していることが明らかになりました(図5参照)。またこの結果は、イメージング技術を用いない別の測定法である液体クロマトグラフィー‐質量分析法(LC-MS/MS)(注8)を用いた手法でも同様の結果であり、本研究の結果の妥当性を確認しました。
本研究では、サイクリックイオンモビリティー‐質量分析法を質量分析イメージング(可視化)に応用することで、既存のイオンモビリティー質量分析イメージングでは不可能であったリン脂質sn位置異性体の脳内分布を解析し、DHA(22:6)を特定の位置にもつリン脂質が脳内で異なる分布を示すことを明らかにしました。さらに、この手法を用いることで、食事から摂取されたDHAが脳に取り込まれ、脂肪酸の結合位置が異なるリン脂質として、聴覚に関与する下丘など、特定の脳領域に蓄積する可能性も示唆されました。本研究により、これまで見分けることが難しかった脂質構造の違いを可視化し、食事由来脂肪酸の脳内での行先を詳しく調べる新しい研究アプローチが可能になりました。
今後の展開
今回開発した手法は、従来の質量分析では区別することが難しかった、質量が同じで構造のよく似た化合物を分離しながら組織内分布を可視化できる点に特徴があります。本研究ではリン脂質のsn位置異性体を対象としましたが、この技術は同様に分離が困難なさまざまな生体分子の解析にも応用できる可能性があります。
本手法を用いることで、生体内における化合物の存在形態や体内動態、作用機序の理解がこれまで以上に精密に進むことが期待されます。特に、DHAの脳内取り込みや代謝変換の解析においては、分子種レベルでの分布を直接可視化できる新しい研究基盤となります。今後、本技術が多様な分子の解析へと展開されることで、栄養科学や脳科学をはじめとする生命科学分野の研究発展に貢献することが期待されます。
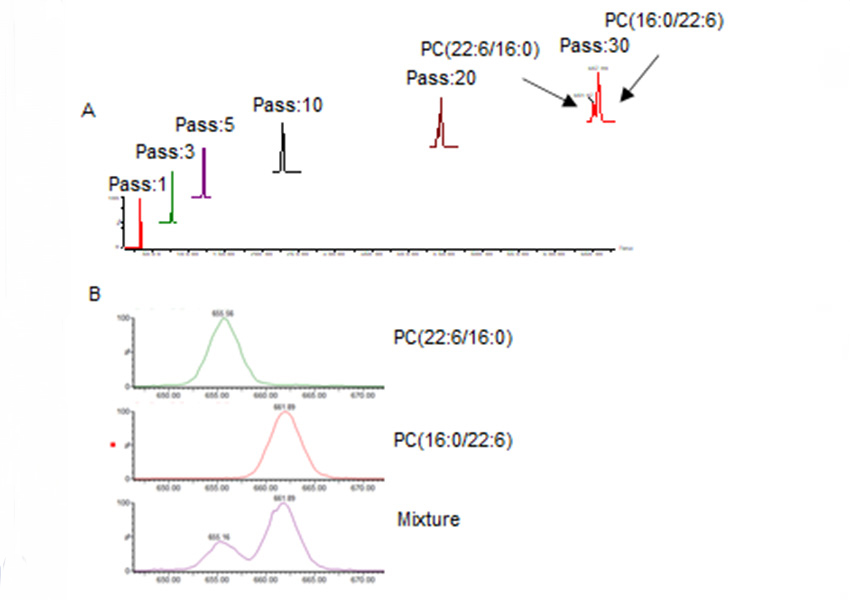
A:PC(22:6/16:0)とPC(16:0/22:6)の混合標準品を用いたサイクリックイオンモビリティーの各周回ごとの分離パターン
B:30周後の分離パターン(拡大図)
図2で示した環状セルの部分で30周することで、PC(22:6/16:0)とPC(16:0/22:6)の異性体が分離し、 PC(22:6/16:0)、PC(16:0/22:6)の順で検出されることが確認できました。
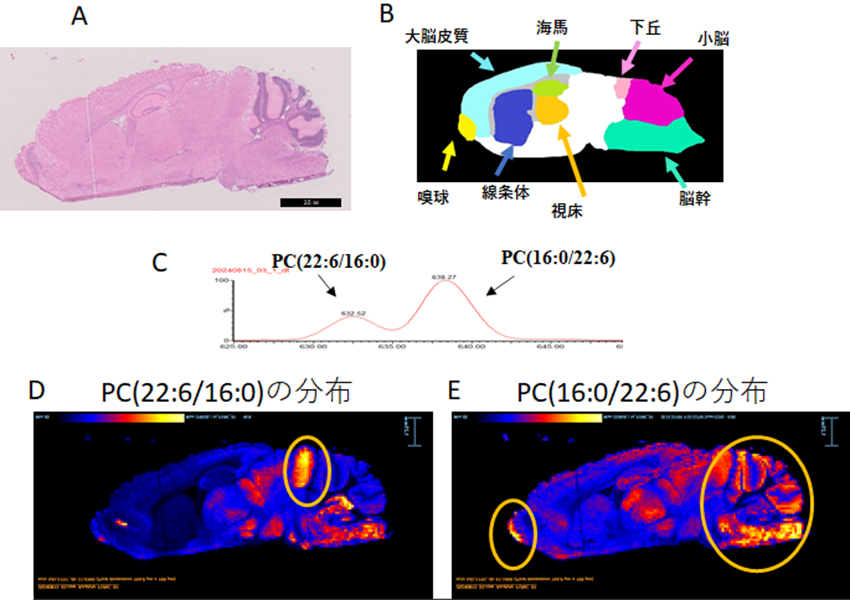
A:マウス脳の組織染色画像
B:マウス脳の各部位の名称
C:PC(22:6/16:0)とPC(16:0/22:6)の分離度を表すモビリグラム(分離パターン)
D:PC(22:6/16:0)の脳内分布 下丘に局在
E:PC(16:0/22:6)の脳内分布 嗅球と小脳、脳幹に広範囲に分布
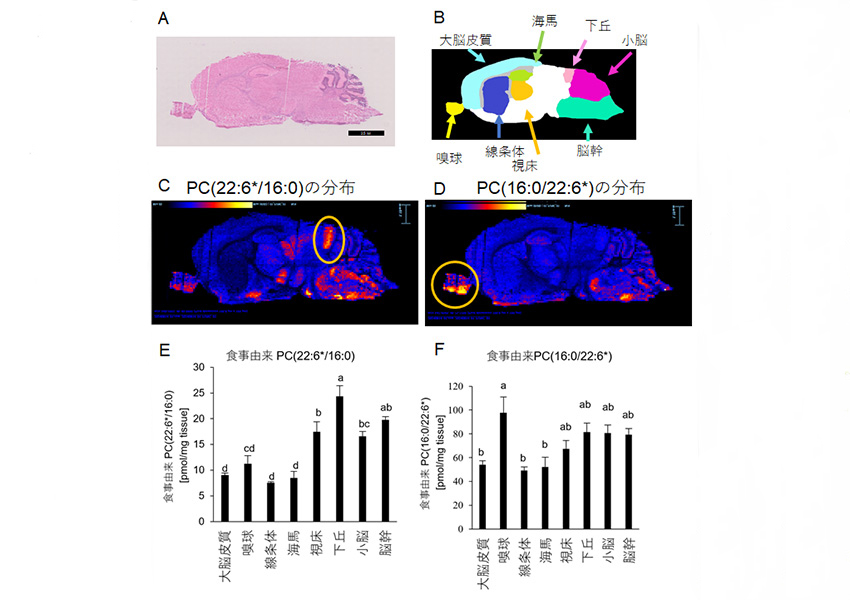
A: マウス脳の組織染色画像
B: マウス脳の各部位の名称
C: PC(22:6*/16:0)の脳内分布 下丘に局在
D: PC(16:0/22:6*)の脳内分布 嗅球に局在
E: LC-MS/MSを用いたPC(22:6*/16:0)の脳部位別の定量結果
F: LC-MS/MSを用いたPC(16:0/22:6*)の脳部位別の定量結果
食事性DHA(22:6*)が取り込まれたPC(22:6*/16:0)とPC(16:0/22:6*)も明確に脳内の分布が異なっていました。
用語解説
(注1):ドコサヘキサエン酸
Docosahexaenoic acid (DHA)とも呼ばれ、魚に豊富に含まれる多価不飽和脂肪酸の一種である。炭素数22個、二重結合6個を持つことから、22:6とも表される。最近アルツハイマー病予防をはじめとする脳機能や老化予防作用があると注目されている脂肪酸である。すでにサプリメントなどにも利用されている。
(注2):リン脂質
ヒトや動物を構成する細胞のしきり部分である細胞膜を構成する成分であり、sn-1位とsn-2位という水酸基(OH基)に脂肪酸がエステル結合し、sn-3位にリン酸やホスホコリンなど、親水性の官能基が結合したもの。脳の主要な脂質である。代表的なリン脂質にホスファチジルコリン(PC)がある。
(注3):sn位置異性体
リン脂質は2つの脂肪酸がsn-1位とsn-2位にエステル結合しており、例えばパルミチン酸(16:0)とDHA(22:6)が結合していたホスファチジルコリンは、PC(16:0/22:6)やPC(22:6/16:0)と表される。このようにPC(sn-1/sn-2)のように結合している脂肪酸の位置を区別して表記する。一般に22:6はsn-2位に結合しやすいため、PC(16:0/22:6)がメインであるが、22:6がsn-1位に結合したPC(22:6/16:0)も構造としては想定され、両者をsn位置異性体と呼ぶ。
(注4):サイクリックイオンモビリティー‐質量分析イメージング
質量分析計を用いたイメージング手法の一つで、イオンモビリティーというイオンの大きさや、かさ高さをもとに分離する部分を有しており、その部分が環状になることで、分離度と呼ばれる分離効率をさらに高めた手法のこと。これにより質量分析イメージングの弱点である、質量が同じ場合に区別できない点を補完できる。
(注5):ホスファチジルコリン(PC)
体内の中で最も豊富なリン脂質であり、sn-1位と2位に脂肪酸が結合し、sn-3位にホスホコリン(リン酸とコリンが結合)が結合した化合物である。脳ではPC(22:6/16:0)とPC(16:0/22:6)で表されるホスファチジルコリンsn位置異性体が存在する。
(注6):下丘
脳の中でも中脳に位置し、聴覚に関わる脳領域である。DHAの同位体を用いた実験でも下丘により多くのDHAが取り込まれたことを報告されている。
(注7):安定同位体
自然界に存在するが、通常の元素よりも重さが異なる元素であり、放射性同位体と比較すると放射線を出さないことから安定であり、かつ扱いやすい同位体である。化学的性質は通常の元素と同様である。今回の場合、DHAの安定同位体を用いることで、体内に元々存在するDHAと、摂取させた安定同位体標識DHAを明確に区別して解析ができる点が優れている。
(注8):液体クロマトグラフィー‐質量分析法(LC-MS/MS)
動物組織の脂質分析で最も一般的に用いられている手法のことで、通常、組織から脂質抽出をして、その脂質を分析する。液体クロマトグラフィーという部分で、化合物の性質により分離した上で、質量分析部分で測定する化合物の重さをベースに検出する手法。質量分析イメージングと比較すると、クロマトグラフィーという分離部を持つことから、より精密で他の化合物の影響を受けづらい分析が可能である。
論文タイトル
“Resolving sn-Positional Isomers of Docosahexaenoic Acid-Bound Phospholipids in the Mouse Brain by Cyclic Ion Mobility Mass Spectrometry Imaging”
(サイクリックイオンモビリティー‐質量分析イメージングを用いたドコサヘキサエン酸が結合したリン脂質のsn位置異性体の分離)
Anal. Chem. 2026, 98, 12, 8966–8975
著者:田中 誠也1、佐々木 映海1、川瀬 泰司2、パクストン タナイ2、廣瀬 賢治2、桐明 絢3、吉永 和明3、岩崎 雄吾4、後藤 直宏1、益田 勝吉5
- 東京海洋大学学術研究院 食品生産科学部門
- 日本ウォーターズ
- 福島大学食農学類
- 中部大学応用生物学部
- 大阪大学理学研究科
DOI:10.1021/acs.analchem.5c06621
https://doi.org/10.1021/acs.analchem.5c06621
研究助成
本研究は、JSPS科研費 若手研究(JP21K17658, JP23K16767)の支援により実施されました。
機関の情報
国立大学法人東京海洋大学(東京都港区港南4丁目5番7号、学長 井関 俊夫)
2003 年に東京商船大学と東京水産大学が統合し設立された国内唯一の海洋系大学。海洋に特化した大学であるという特色を活かし、「海を知り、海を守り、海を利用する」をモットーに、海洋分野におけるグローバルな学術研究の強力な推進とその高度化に取り組んでいます。
お問い合わせ
研究に関すること
岩崎 雄吾(イワサキユウゴ)中部大学 応用生物学部 応用生物化学科 教授
Tel:0568-51-9336
E-mail:iwasaki[at]fsc.chubu.ac.jp ※アドレスの[at]は@に変更してください。
取材に関すること
中部大学 入試・広報センター
Tel:0568-51-5541
E-mail:chubu-info[at]fsc.chubu.ac.jp ※アドレスの[at]は@に変更してください。