1. ポイント
- 次世代燃料(FFA)を高生産する微細藻類を開発:ジェット燃料やディーゼル燃料の原料となる遊離脂肪酸(FFA:Free Fatty Acid)(1)を効率よく作り出す微細藻類の開発に成功しました。
- 「細胞外放出」による革新:生産したFFAを細胞の外へ排出させることで、従来の課題だった藻類の「回収・乾燥・抽出」工程を簡略化。回収エネルギーの大幅な削減、細胞体積を超える連続生産、細胞残さの低減を可能にしました。
- 社会実装を見据えた「セルフクローニング(2)」:外来遺伝子を残さない手法を採用したため、遺伝子組換え規制の枠外(セルフクローニング)として、産業利用に向けた高い優位性を持っています。
- カーボンニュートラル:光合成(3)により大気中のCO2から燃料物質を直接合成するため、脱炭素社会の実現に大きく貢献する技術です。

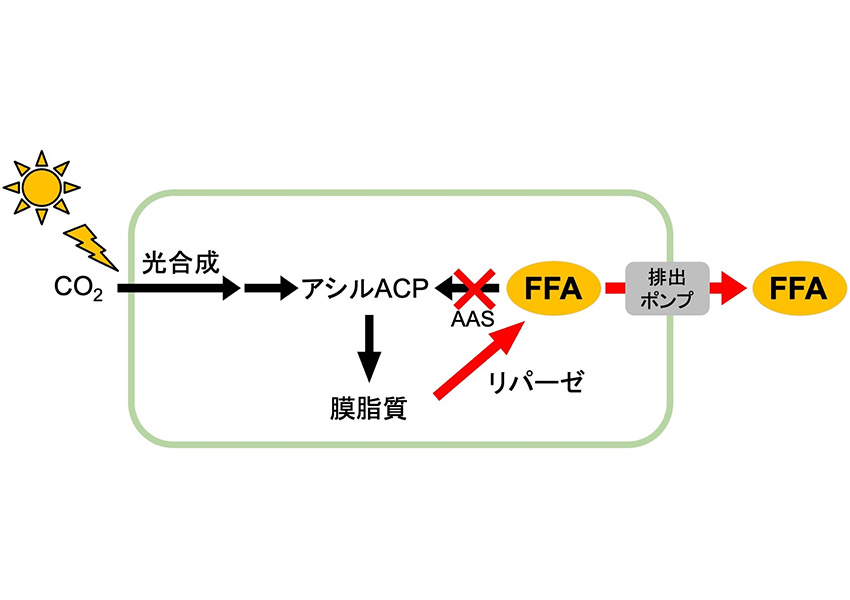
- ラン藻Synechococcus elongatus をもとに、アシルACP合成を抑制し、排出ポンプとリパーゼの働きを強化しました。
2. 概要
埼玉大学大学院理工学研究科の西山佳孝教授らの研究グループは、大成建設株式会社の山本哲史チームリーダー、中部大学の愛知真木子准教授、かずさDNA研究所の池田和貴グループ長らと共同で、バイオ燃料の原料となる遊離脂肪酸(FFA)を、光合成によって細胞外へ効率よく放出する革新的なラン藻(4)(微細藻類)を開発しました。本研究では、細胞内の膜脂質を分解する酵素「リパーゼ」と、脂肪酸を細胞外へ汲み出す「RND型ポンプ(5)」という、藻類が本来持っている遺伝子の働きを強化する「セルフクローニング技術」を用いました。これにより、外来遺伝子を含まない、産業利用に最適な「生きた燃料工場」を実現しました。本成果は、バイオ燃料の生産・回収コストを劇的に抑え、カーボンニュートラル社会の実現を加速させるものとして期待されます。
本成果は、2026年4月30日にバイオテクノロジー関連の専門誌『Biotechnology for Biofuels and Bioproducts』のオンライン版で公開されました。
3. 研究の背景:実用化への「遺伝子組換え」と「コスト」の壁
微細藻類によるバイオ燃料生産は、食料生産と競合しない脱炭素エネルギーとして注目されています。しかし、従来の手法には3つの大きな課題がありました。
- 回収エネルギーの過大:多くの藻類は燃料物質(トリアシルグリセロールなど)を細胞内に貯めるため、燃料を取り出すには大量の細胞を回収・乾燥して抽出する必要があり、生産エネルギーの半分以上をこの工程に消費していました。
- 細胞残さの問題:燃料物質を細胞内に高蓄積する藻類の場合、燃料物質の占める割合は最大でも細胞体積の50%ほどになります。つまり、燃料物質をすべて取り出すことができても、それと等量以上の細胞残さ(細胞のカス)が残ってしまいます。
- 法規制による制限:生産能力を高めるために大腸菌などの外来遺伝子(例:tesA)を導入すると、「カルタヘナ法(6)」などの厳しい規制対象となり、屋外の大規模な培養施設での利用が困難でした。
研究グループは、藻類自身が持つ「脂質を分解して外へ出す」能力に着目し、外来遺伝子に頼らない手法での課題解決に挑みました。
4. 研究の内容:自給自足の「排出システム」を構築
本研究では、淡水性ラン藻 Synechococcus elongatus を対象に、以下の3つの機能を独自のセルフクローニング技術で強化し(図2)、FFA生産条件を最適化しました。
【機能強化】
- アシルACP(7)合成の抑制:ラン藻は本来自身の膜脂質を利用してFFAを生成していますが、FFAをアシルACPに変換して再利用しています。そこでまず、アシルACP合成酵素(AAS)の遺伝子を破壊し、アシルACPの合成を抑制しました。
- 「汲み出し機能」の促進:生成したFFAは細胞に毒性を示すため、これを速やかに外へ汲み出す「RND型ポンプ」を過剰発現させました。
- 「膜脂質の分解」の強化:膜脂質を分解してFFAを作る酵素(ガラクトリパーゼ(8):LipBおよびLipC)を過剰発現させました。
【培養の最適化】
- 二相培養法によるFFAの回収:放出されたFFAを培養液に重ねた有機溶媒へ自動的に回収することで、細胞を死なせることなく燃料物質を継続して得ることができました。
- 強光ストレスと低温ストレス(9)の活用:強光ストレスに加え、本来の最適温度(32℃)よりも低い25℃で培養することで、細胞あたりのFFA生産性が劇的に向上することを発見しました。
【FFA生産性】
- 開発したセルフクローニング株は、FFA生産量(389 ± 48 mg/L)、FFA生産速度(0.81 ± 0.10 mg/L/h)、乾燥細胞重量あたりのFFA生産速度(24.7 ± 5.8 mg/g-(DCW)/day)、FFA/乾燥細胞重量比(0.49 ± 0.12 g/g)を示し、高い生産性を達成しました。
5. 今後の展開:脱炭素燃料の社会実装へ
本研究の成果は、以下の点で藻類バイオ燃料の開発に貢献します。
- 細胞外生産:バイオ燃料の生産が細胞キャパシティの制限を受けないため、細胞体積を超えた燃料の連続生産が可能です。
- 低コスト生産:細胞外生産による燃料回収の簡略化に加え、低温(25℃)で高い生産性を示すため、培養・回収工程のエネルギーとコストを大幅に削減できます。
- 屋外大規模培養の実現:外来遺伝子を含まない「セルフクローニング株」であるため、法規制のハードルが低く、広大なオープンポンド(培養池)での利用が現実的になります。
- 今後は、セルフクローニング株のさらなる改良や、安価なFFA回収方法の開発、実際の屋外環境(太陽光や気温の変化)における生産の最適化を進め、ジェット燃料やディーゼル燃料などの持続可能な燃料供給源としての確立を目指します。
6. 論文情報
| 雑誌名 | Biotechnology for Biofuels and Bioproducts |
| 論文名 | Overexpression of endogenous galactolipases and an efflux transporter enhances the secretion of extracellular free fatty acids by Synechococcus elongatus PCC 7942 (Synechococcus elongatus PCC 7942のガラクトリパーゼと排出トランスポーターの過剰発現による遊離脂肪酸の細胞外排出の促進) |
| 著者 | Kotoha Nishimoto, Tsubasa Furushima, Taro Kadowaki, Haruhiko Jimbo, Norifumi Yamamoto, Kazutaka Ikeda, Nobuyuki Takatani, Makiko Aichi, Tatsuo Omata, Yoshitaka Nishiyama* (*責任著者) |
| DOI | 10.1186/s13068-026-02768-0 |
| URL | https://link.springer.com/article/10.1186/s13068-026-02768-0 |
7. 研究支援
本研究は、NEDO(国立研究開発法人新エネルギー・産業技術総合開発機構)「カーボンリサイクル実現を加速するバイオ由来製品生産技術の開発」(JPNP20011)、文部科学省科学研究費助成事業(科研費)学術変革領域研究(A)「ジオラマ環境で覚醒する原生知能を定式化する細胞行動力学(ジオラマ行動力学)」(21H05305)、科研費・学術変革領域研究(A)「あらゆる地球環境で光合成を可能とする超分子構造制御(光合成ユビキティ)」(24H02066)、科学技術振興機構(JST)COI-NEXT「Bio-Digital Transformation(バイオDX)産学共創拠点」(JPMJPF2010)、物質・デバイス領域共同研究拠点の支援を受けて行われました。
8. 用語解説
(1)遊離脂肪酸(FFA:Free Fatty Acid)
脂質の構成成分。ジェット燃料やディーゼル燃料(軽油代替)の直接の原料となる物質。
(2) セルフクローニング
対象とする生物自身、またはその近縁種の遺伝子のみを利用して育種する手法。外来遺伝子を一切残さないため、多くの国で遺伝子組換え規制の対象外、あるいは緩和された基準が適用されます。
(3) 光合成
光エネルギーを使って二酸化炭素と水から糖を生産する一連の反応。植物や藻類、ラン藻などの光合成生物にとって生存上欠かすことのできない重要な生命活動です。また、光合成によって作られた糖は、地球上のすべての生命の炭素源となっています。光合成反応で生み出される酸素は、大気の約21%を占める酸素層を形成しており、人類を含む地球上のすべての好気生物の呼吸を支えています。
(4) ラン藻
植物葉緑体の祖先と考えられている原核性の光合成微生物。シアノバクテリアとも呼ばれます。約27億年前に地球上に誕生し、酸素を発生する光合成を初めて行なったと考えられています。現在もほぼ昔の姿をとどめ、湖沼や海洋に生息しています。ラン藻の一種Synechococcus elongatus は、ゲノムが解読され、形質転換(遺伝子操作)も容易なことから、モデル生物として光合成研究などに世界中で利用されています。
(5) RND型ポンプ
耐性-根粒形成-細胞分裂(Resistance-Nodulation-cell Division)型ポンプ。細胞内から細胞外へ特定の物質を能動的に排出するタンパク質。本研究では脂肪酸の汲み出しを担い、細胞内の毒性を低減させています。
(6) カルタヘナ法
遺伝子組換え生物等の使用を規制し、生物多様性を守るための国際的な枠組み(および国内法)。外来遺伝子を持つ生物を環境中で扱うには、非常に厳しい承認手続きが必要です。
(7) アシルACP
アシル基運搬タンパク質(ACP:Acyl Carrier Protein)にアシル基が結合した物質で、脂肪酸合成の反応中間体。膜脂質から切り出された脂肪酸FFAはACPに再結合し、リサイクルされます。
(8) ガラクトリパーゼ
ラン藻の生体膜を構成する「ガラクト脂質」を分解し、脂肪酸を切り出す酵素。LipBおよびLipCは近年、中部大らのチームによりラン藻で同定されたガラクトリパーゼです。
(9) 強光ストレスと低温ストレス
最適生育条件よりも、強い光や低い温度といったストレス条件で、リパーゼが活性化されることが中部大らのチームにより明らかにされています。
お問い合わせ
研究について
愛知 真木子 中部大学応用生物学部応用生物化学科准教授
TEL:0568-51-6194
e-mail:makiko[at]fsc.chubu.ac.jp ※アドレスの[at]は@に変更してください。
報道について
中部大学 入試・広報センター
TEL:0568-51-5541
e-mail:chubu-info[at]fsc.chubu.ac.jp ※アドレスの[at]は@に変更してください。